“Meu nome é Timothy Ray Brown e sou a primeira pessoa no mundo a ser curada do HIV.” Foi com essa simples — e histórica — apresentação que o homem conhecido como “paciente de Berlim” iniciou um artigo publicado em 2015 no periódico Aids Research and Human Retroviruses, em que relatava o sucesso da terapia que inaugurou um ciclo de esperança para a cura de um dos vírus mais complexos já enfrentados pela ciência. Em 2007, seu organismo foi declarado livre do HIV, causador da síndrome da imunodeficiência adquirida, a aids, após um transplante de células-tronco de um doador com rara mutação que torna as células resistentes ao vírus. Entre 2019 e 2022, outros quatro casos foram anunciados e, no último dia 20 de fevereiro, um novo episódio de remissão — do “paciente de Düsseldorf”, desta vez — pode ter consolidado o método como alternativa para chegar à vitória contra a infecção que afeta 38,4 milhões de pessoas.
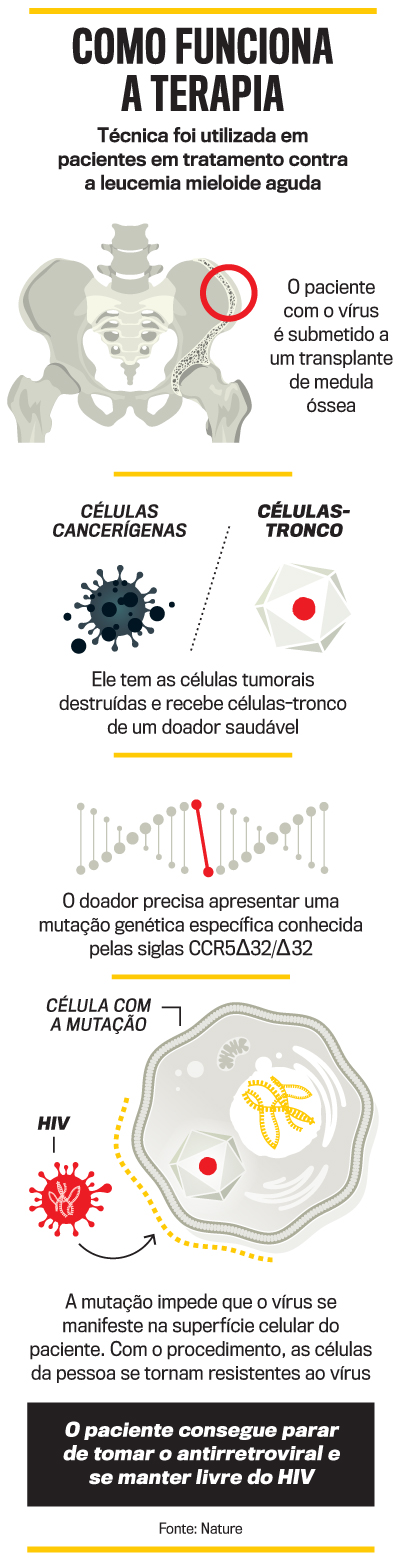
Assim como os demais casos de cura, o de agora foi submetido ao tratamento de um câncer no sangue e na medula óssea, a agressiva leucemia mieloide aguda. A chave para o sucesso é a troca das células tumorais por outras com uma mutação que impede a proliferação do vírus no organismo mesmo em pacientes que fazem a terapia antirretroviral e apresentam carga viral indetectável. Embora a ciência tenha reduzido os efeitos colaterais e a quantidade de medicações daquilo que um dia foi chamado de “coquetel anti-aids”, o desafio continua sendo extirpar o vírus dos hospedeiros humanos.
A tarefa é hercúlea pelo fato de se tratar de um rival cheio de artimanhas. O HIV é um vírus com duas cepas, 1 e 2, além de ao menos nove subtipos, e apresenta mutações consideradas lentas — ao contrário do novo coronavírus, causador da Covid-19. Mutar menos e estar sob controle com remédios não o torna menos ardiloso. Ele permanece latente e escondido em lugares que a medicina denominou como “reservatórios”. Lá, o vírus se mantém pronto para subjugar as células de defesa e iniciar sua trajetória de destruição se as terapias forem interrompidas. Por isso, é considerado incurável de forma geral. “Ele fica adormecido no sistema nervoso central, nos linfonodos e nas mucosas do trato gastrintestinal e geniturinário”, diz José Valdez Madruga, coordenador do Comitê de HIV-Aids da Sociedade Brasileira de Infectologia.
Com o transplante de células-tronco, o vírus depara com células resistentes à infecção, o que permite a interrupção do tratamento sem que o HIV se manifeste nem apareça adormecido em testes novamente. O “paciente de Düsseldorf”, um homem de 53 anos, não toma antirretrovirais desde 2018. Até morrer de leucemia, em 2020, Timothy Ray Brown, aquele de Berlim, não fazia uso dos medicamentos, assim como “o paciente de Londres”, Adam Castillejo, curado em 2019. O microbiologista Ravindra Gupta, da Universidade de Cambridge, no Reino Unido, esteve à frente dos cientistas que atuaram no caso de Castillejo e acredita que a ciência está preparando o terreno para novos avanços. “Cada caso que descrevemos oferece condições para demonstrar isso”, disse a VEJA.

O cuidado dos especialistas com as expectativas elevadas sobre a cura definitiva se deve ao fato de não ser possível, ainda, imaginar a oferta em larga escala do método. Além de a mutação fundamental para o procedimento ser rara — está presente em menos de 1% da população mundial —, há a necessidade de um diagnóstico de leucemia. Sem contar que o transplante é perigoso. “Um paciente com leucemia submetido ao transplante pode ter um risco de morte de quase 50%”, diz o infectologista Rico Vasconcelos, pesquisador da Faculdade de Medicina da USP. “Não faz sentido expor uma pessoa saudável a um procedimento tão letal.” O próprio Brown fez o transplante duas vezes e, na segunda, em 2008, sofreu com cegueira parcial e perda de movimentos. Ele se recuperou do quadro seis anos depois, após reabilitação em uma clínica especializada em lesões cerebrais.

Os especialistas contam com outras armas para combater o vírus. “É possível pensar em drogas e vacinas para tornar as células resistentes às infecções e em tratamentos para modificar os genes”, afirma Gupta. Enquanto isso, os cientistas trabalham no aprimoramento do arsenal desenvolvido nas últimas décadas. São diferentes frentes, da prevenção ao tratamento, e com métodos que consideram, sem julgamentos, o comportamento sexual de cada um, tendo em vista os avanços alcançados para evitar a transmissão por transfusão de sangue, da mãe para o bebê e por objetos perfurantes em procedimentos hospitalares. Em dezembro passado, a droga lenacapavir foi aprovada pela agência reguladora americana Food and Drug Administration (FDA) para a proteção da população que vive com o HIV. O estudo clínico que embasou a aprovação indicou que 83% dos voluntários multirresistentes a drogas alcançaram a carga viral indetectável em um ano de tratamento.
Retirar os medicamentos diários e avançar para opções injetáveis espaçadas também são métodos vislumbrados para os demais pacientes. Na semana passada, durante a 30ª Conferência sobre Retrovírus e Infecções Oportunistas (CROI), foi apresentado um ensaio apontando que o regime injetável com os fármacos cabotegravir e rilpivirina a cada dois meses tem os mesmos benefícios de um tratamento padrão com pílulas diárias. O ponto positivo da proposta é o conforto emocional para os pacientes. Para 47% dos 447 voluntários do estudo Solar, espaçar as doses aplaca o medo de ter seu status sorológico descoberto por colegas.
As conquistas da medicina nos últimos anos ajudaram a combater os estigmas que sempre acompanharam os pacientes que vivem com HIV. Campanhas informativas lançadas em diversos países, inclusive no Brasil, e a luta pertinaz de milhares de pessoas que foram às ruas gritar contra o preconceito também levaram a infecção a ser enfrentada com mais dignidade. Ainda assim, ela avança. No Brasil, 52 000 jovens de 15 a 24 anos com HIV evoluíram para aids entre 2011 e 2021, dado alarmante diante da possibilidade de evitar o crescimento da doença com medicamentos distribuídos gratuitamente. Enquanto não surgir a cura, a sociedade deveria se engajar para combater a ignorância — e para ela, infelizmente, também não há vacina.
Publicado em VEJA de 8 de março de 2023, edição nº 2831


 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO


 Greves e manifestações param a França contra reforma da Previdência
Greves e manifestações param a França contra reforma da Previdência Marçal ultrapassa Nunes e encosta em Boulos em nova pesquisa AtlasIntel
Marçal ultrapassa Nunes e encosta em Boulos em nova pesquisa AtlasIntel MPT abre investigação contra Silvio Almeida por assédio sexual
MPT abre investigação contra Silvio Almeida por assédio sexual Albert Einstein cria iniciativas contra obesidade de colaboradores
Albert Einstein cria iniciativas contra obesidade de colaboradores Na Espanha, empresas de cigarro serão obrigadas a limpar bitucas das ruas
Na Espanha, empresas de cigarro serão obrigadas a limpar bitucas das ruas





![[BF2024] - Paywall - DESKTOP - 728x90](https://gutenberg.veja.abril.com.br/wp-content/uploads/2024/10/BF2024-Paywall-DESKTOP-728x90-1.gif)
![[BF2024] - Paywall - MOBILE - 328x79](https://gutenberg.veja.abril.com.br/wp-content/uploads/2024/10/BF2024-Paywall-MOBILE-328x79-1.gif)


